Agromining: planten delven ertsen
Het proces om geselecteerde planten als hyperaccumulatoren van metalen in de bodem te telen heet phytomining (door mijnbouwers) of agromining (als landbouwers het doen). Hyperaccumulatoren verdragen hogere concentraties die giftig zijn voor de meeste andere planten. Stekken van houtige planten worden gedroogd en verbrand tot as die bio-erts wordt genoemd. Ook nieuwe termen als metaalboerderij en metaalgewas worden door deze activiteiten gelanceerd.
De techniek is bruikbaar om vervuilde gronden te reinigen en om metaal te oogsten.
Sommige hyperaccumulatoren gedijen vooral op nikkel, maar ook op kobalt, zink en zelfs goud.
Wetenschapper Alan Baker ontdekte dat het jadegroene fluorescerende sap van de Filippijnse Phyllanthus Balgooyi voor 9% uit nikkel bestaat. Hyperaccumulator Sebertia acuminata wordt commercieel gebruikt voor Ni-fytomining en kan sap produceren met maximaal 25% Ni op gewichtsbasis. Dat is veel geconcentreerder dan het erts dat nikkelsmelterijen gebruiken.
In Maleisië runt de Universiteit van Lorraine al vijf jaar een metaalboerderij, met opbrengsten van tussen de 200 en 300 kilogram nikkel per hectare per jaar.
Met (Ni) hyperaccumulator Streptanthus polygaloides kon een opbrengst van 100 kg/ha zwavelvrij Ni geproduceerd worden. Ni-hyperaccumulatoren Alyssum bertolonii (Italië) en Berkheya coddii (Zuid-Afrika) hebben een nog groter potentieel, meer dan 20 t/ha met een Ni-concentratie van 1% in de droge stof.
In Eurazië worden vooral Alyssum murale (Albanië, 100 kg nikkel/ha), Leptoplax emarginata en Bornmuellera tymphaea (in Griekenland) gebruikt.
De meeste (vooral zware) metalen zijn giftig, vooral in overdosering. Metaal concentreert vooral in bladeren en bloemen.
Bij de Macadamia-boom zijn de bladeren en het sap, maar niet de noot, rijk aan mangaan.
Bij Iberis intermedia en Biscutella laevigata (Brassicaceae) uit Zuid-Frankrijk is een ongebruikelijke hyperaccumulatie (>500 mg/kg droge massa) van thallium (Tl) vastgesteld.
Het meerjarige Ocimum centraliafricanum (koperbloem of koperplant, Centraal-Afrika) verzamelt hoge concentraties koper en wordt door geologen gebruikt om edele metalen te zoeken.
Een lixiviant is vloeistof die in de hydrometallurgie gebruikt wordt om selectief een gewenste metaal uit erts of mineraal te extraheren. Het helpt bij een snelle en volledige uitloging. Toegevoegde lixivianten hebben Brassica juncea ertoe aangezet goud te accumuleren tot concentraties van meer dan 100 mg/kg op basis van droge stof.
Snelle groeiers presteren (verzamelen) meestal beter. Er wordt dus ook nogal wat stimulerend kunstmest en extra kalk gebruikt. Een terechte vraag lijkt me: na hoeveel oogsten is het land leeggezogen?
Moet er naast de economische haalbaarheid ook geen onderzoek gedaan worden naar de ecologisch impact van het gehele proces?
Zie ook Geobotanie: plant verklikt ondergrond; Fytoremediatie: planten saneren de bodem
Geobotanie: plant verklikt ondergrond
Geobotanica is de wetenschap die de samenhang tussen de geografie en de plantengroei bestudeert. Daarbij inbegrepen de relatie tussen planten en (ondergrondse) mineralen. Het gebruik van planten om ertsen te vinden heet geobotanische prospectie. Ook voor olie en gas exploratie, boren, teerzand en olieschalie mijnbouw.
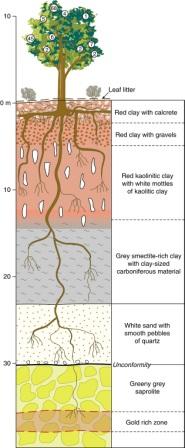 De Chinezen hebben geobotanische beschrijvingen die stammen van enkele honderden jaren voor onze jaartelling. Ze gebruikten deze kennis om metalen te zoeken.
De Chinezen hebben geobotanische beschrijvingen die stammen van enkele honderden jaren voor onze jaartelling. Ze gebruikten deze kennis om metalen te zoeken.
Viola calaminaria en vooral Boerenkers (Thlaspi) zijn zinkminnend.
Schildzaad (Alyssum bertolini) kon tegen hoge concentraties nikkel.
Gierstgras (Panicum crusgalli) duidt op aanwezigheid van lood.
Duizendknoop houdt van hematiet (ijzeroxide).
Grove bieslook lust zilver.
Gember staat op koper en tin.
Siai en hwéi-t’ang duidt op gouderts. En daarvan werd er natuurlijk geen vertaling gevonden.
Geen van deze oude Chinese aanwijzingen is bij mijn weten getest of bewezen. Een wetenschappelijk terrein waarop blijkbaar nog heel veel werk te doen is.
De Viscaria Mijn in Zweden is genoemd naar de bloem Viscaria Alpina, gebruikt door prospectors om de erts afzettingen te ontdekken.
Een betrouwbare indicator plant is Ocimum centraliafricanum, de "koperplant" (of – bloem), die alleen op koper (en nikkel) bevattende bodems in centraal Zuid-Afrika voorkomt.
Koper en nikkel accumuleert ook in Helichrysum candolleanum en Blepharis diversispina.
De Alpen Koekoeksbloem (Lychnis alpina) met roze bloemen wordt sinds de middeleeuwen gebruikt om koper te vinden. Modern onderzoek heeft ontdekt dat de soort genetisch resistent is tegen het metaal, zodat ze gedijt in de bodem waar de aanwezigheid van kopererts andere planten het leven onmogelijk maakt.
Pandanus candelabrum is een tot 10 meter hoge palmachtige met een bovengrondse wortelstelsel vergelijkbaar met dat van mangrovebomen. Ze groeit op kimberlietrijke bodem, met een hoog gehalte aan magnesium, kalium en fosfor. Die komen voor in verticale pijpen van vulkanisch gesteente met een doormeter van honderden meters. Waar deze boom groeit kan er diamant gevonden worden. Er zijn zo ongeveer 6000 plaatsen bekend op de wereld. Slechts ongeveer 600 daarvan bevatten diamanten, en bij slechts 60 zijn dat voldoende edelstenen om er aan mijnbouw te doen.
Zware metalen accumuleren in Rumex acetosella L. (schapenzuring) en Minuartia verna (L.) (zinkveldmuur).
Er zijn ook projecten om zware metalen te accumuleren en te extraheren.
Ik neem aan dat planten zich over generaties ook regionaal aanpassen, en dat hun voorkomen niet overal op dezelfde (hoeveelheid) aanwezige metalen/mineralen wijst.
Een verbazingwekkend voorbeeld is de westelijke spiderwort (Tradescantia occidentalis): de blauwe meeldraden in de bloemen worden roze als er straling in de omgeving aanwezig is.
Het zout der aarde NaCl e.a.
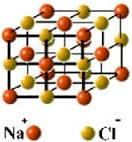 Een zout is een chemische verbinding van positieve (kationen) en negatieve ionen (anionen), die door elektrostatische aantrekkingskracht verbonden zijn. Het is in vaste aggregatietoestand een kristallijne stof waarin de positieve en negatieve ionen in een kristalrooster zijn gerangschikt. In omgangstaal wordt met zout meestal keukenzout (natriumchloride of NaCl) bedoeld.
Een zout is een chemische verbinding van positieve (kationen) en negatieve ionen (anionen), die door elektrostatische aantrekkingskracht verbonden zijn. Het is in vaste aggregatietoestand een kristallijne stof waarin de positieve en negatieve ionen in een kristalrooster zijn gerangschikt. In omgangstaal wordt met zout meestal keukenzout (natriumchloride of NaCl) bedoeld.
Veel vaste stoffen hebben een kristalstructuur, ze bestaan uit een regelmatig patroon (rooster) van moleculaire, atomaire of ionaire structuureenheden, die de bouwstenen van een kristal vormen.
Kristalstructuren worden gekenmerkt door hun symmetrie.
Naast kristallijne vaste stoffen bestaan er glasstructuren (niet gekristalliseerde stolling) en amorfe structuren. Deze laatste zijn niet vloeibaar en niet kristallijn, vb. suikerspin, bijenwas, paraffine, barnsteen, opaal, polymeren als polystyreen...
In ons lichaam vindt voortdurend assimilatie (opbouw) en dissimilatie (afbraak) van verbindingen plaats. Dit heet stofwisseling.
Vroeger werd er in de alchemie gezocht naar manieren om metalen te transformeren (in goud).
Veel stoffen kunnen nuttig gebruikt worden als ze de juiste samenstelling (en concentratie) hebben.
‘Geleerde: iemand die alles weet van wat de anderen niet weten,
en niets weet van wat de anderen wel weten.’
(Albert Einstein)
‘Vandaag de dag zijn de geneesmiddelen zo doeltreffend
dat men ze niet meer kan innemen zonder gevaar voor de gezondheid.’
(Jan Boschmans)
Belangrijke chemische elementen
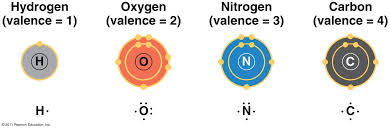 Zuurstof (Latijn: oxygenium, symbool O, atoomnummer 8) is een niet-metaal dat tot de zuurstofgroep in het Periodiek Systeem behoort. Zuurstof komt als enkelvoudige stof vooral als dizuurstof (O2) in de atmosfeer voor. In samengestelde vorm is het wijdverspreid omdat alle water en alle silicaten waar de aardkorst uit bestaat zuurstof bevatten. Naar gewicht is zuurstof het meest voorkomende element in het menselijk lichaam: ongeveer 65 %, voornamelijk in de vorm van water.
Zuurstof (Latijn: oxygenium, symbool O, atoomnummer 8) is een niet-metaal dat tot de zuurstofgroep in het Periodiek Systeem behoort. Zuurstof komt als enkelvoudige stof vooral als dizuurstof (O2) in de atmosfeer voor. In samengestelde vorm is het wijdverspreid omdat alle water en alle silicaten waar de aardkorst uit bestaat zuurstof bevatten. Naar gewicht is zuurstof het meest voorkomende element in het menselijk lichaam: ongeveer 65 %, voornamelijk in de vorm van water.
Stikstof (symbool N, atoomnummer 7) is een niet-metaal uit de stikstofgroep. Losse atomen hiervan zijn zeer reactief en verbinden zich direct met andere stikstofatomen. Hierbij wordt meestal distikstof gevormd (N2 of moleculaire stikstof), de gangbare verschijningsvorm van stikstof. Op kamertemperatuur verkeert N2 in gasvorm.
Waterstof (symbool H (Latijn: Hydrogenium), atoomnummer 1) komt normaal niet in geïsoleerde vorm voor, maar vormt door de hoge reactiviteit verbindingen. Het vormt een twee-atomig molecule: diwaterstof, meestal gewoon waterstof of waterstofgas genoemd. Waterstof is het meest voorkomende element in het universum. Het normale isotoop van waterstof "protium" bestaat maar uit één proton en één elektron en bevat dus geen neutronen. Waterstof is het enige element dat zonder neutronen bestaat.
Koolstof (symbool C, atoomnummer 6) bestaat in verschillende vormen (houtskool, diamant…) en zit o.m. in koolwaterstoffen (fossiele brandstof), koolhydraten (ethanol, suikers, zetmeel…). Alle organische verbindingen bevatten koolstof. (Enkel CO2 en carbonaten worden toch tot de anorganische stoffen gerekend.) Koolstofverbindingen vormen de basis van al het leven op aarde.
Sacharose, suiker: C12H22O11
Glucose C6H12O6 verbrandt > 6CO2(g) + H2O (g) (omgekeerde = fotosynthese)
Aardgas = methaan CH4 verbrandt CO2 en H2O. Ethaan: H3C-CH3.
Koolhydraten: ((CH2O))n
Alcohol: C2H5OH
Zuur (pH laag) loog (pH hoog)
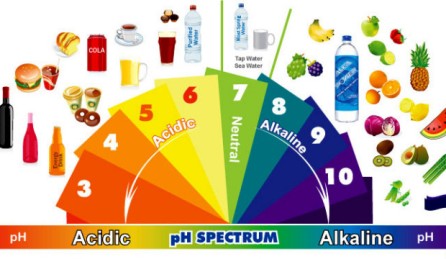 Een zuur is een stof die protonen (H+-ionen) af kan staan. Wat overblijft is de negatieve zuurrest. Zuren zijn de tegenhangers van de basen. Een waterige oplossing wordt zuur genoemd als de pH (zuurtegraad op een schaal van 0 – 14) lager is dan 7. (p=Potenz, H: waterstofion H+)
Een zuur is een stof die protonen (H+-ionen) af kan staan. Wat overblijft is de negatieve zuurrest. Zuren zijn de tegenhangers van de basen. Een waterige oplossing wordt zuur genoemd als de pH (zuurtegraad op een schaal van 0 – 14) lager is dan 7. (p=Potenz, H: waterstofion H+)
De zuurgraad geeft het aantal waterstofionen in een concentratie weer.
Een concentratie van 1 op 10 miljoen = 1/107 = pH 7
Een concentratie van 1 op 1 miljoen = 1/106 = pH 6
Citroenzuur en azijnzuur zijn bekende stoffen die een zure smaak geven. In hoge concentraties, als de pH lager is dan 1 kunnen zuren schadelijk zijn. Een pH lager dan 4,5 is giftig voor verschillende (water)diertjes. Een pH lager dan 1,5 kan brandwonden veroorzaken (huid oplossen).
pH 14: natronloogoplossing van 1 mol/l
pH 13: natronloogoplossing of kaliloogoplossing van 0,1 mol/l
pH 12: ovenreiniger
pH 11,5: huishoudammonia (verdunde ammonia dus)
pH 10,5: zeepsop
pH 9,5: bleekwater
pH 8,5: zeewater, darmsap (iets verhoogde pH door gal)
pH 7,5: eieren
pH 7,4: menselijk bloed
pH 7: zuiver, gedestilleerd water (neutraal), klei en duinzandgrond
pH 6,7: melk
pH 6,5: speeksel
pH 6: natuurlijke regen, urine, zandgronden
pH 5,5: huid
pH 5: licht zure regen, veengrond
pH 4,5: tomaten, druiven
pH 4: zure regen, tomatensap, bier
pH 3,5: appel, sinaasappelsap
pH 3: consumptieazijn, wijn, zuurkool, aalbes
pH 2,8: cola, azijn
pH 2: maagzuur, citroensap
pH 1: zwavelzuur (accuzuur)
pH 0: zoutzuur (1 mol/l), zwavelzuur (1 N)
Onedele metalen als ijzer, zink en magnesium lossen op in zuren (vb. geconcentreerd zoutzuur) onder vrijkomen van waterstofgas.
In geconcentreerd zwavelzuur, salpeterzuur of koningswater lossen ook edele metalen op, omdat zij ook sterke oxidatoren zijn.
Een base of loog in oplossing heeft een pH-waarde hoger dan 7 en zal lakmoespapier blauw kleuren. (Basisch wordt ook alkalisch genoemd.)
Zuren worden door basen geneutraliseerd onder vorming van een zout en water. Zwakke basen, zoals aluminiumhydroxide, kunnen gebruikt worden voor het tijdelijk neutraliseren van maagzuur. Sterke basen zijn even gevaarlijk of nog gevaarlijker dan sterke zuren en veroorzaken ernstige weefselbeschadiging. Een voorbeeld van een sterke base is natronloog.
De zuurgraad bepaalt (de levensvatbaarheid voor) het bodemleven, en de binding en dus ook de beschikbaarheid van mineralen voor bodemleven en planten.
Zelfmedelijden is het zuur dat gaten in geluk vreet.
(Earl Nightingale)
Mensen zijn net als wijn.
naarmate ze ouder worden,
worden sommigen zuur,
en anderen worden beter.
Anthocyaan, de rode stof in rode vruchten en bv rode kool, werd gebruikt als een zuur/base-indicator. Veel natuurlijke kleurstoffen verkleuren ook als de pH verandert. Anthocyaan is roze-rood in een zure omgeving, en blauw, groen en geel in een basische.
Als je bij de stof een zure oplossing ( zoals zoutzuur of azijn) voegt, kleurt de oplossing rood. Met een basische oplossing (zoals natronloog of soda of ammonia) kleurt de stof over blauw en groen, geel. Daarom voegt men bij de bereiding van rode kool een appeltje toet, door het zuur daarvan krijgt de rode kool een aangenamere, lichtere kleur.
Lakmoespapier wordt gemaakt van lakmoes, een plantaardige kleurstof die gehaald wordt uit mossen, vnl. uit Lecanora tartarea en Rocella tinctoria. Het wordt rood als het met zuren in aanraking komt, en blauw als het met een base in contact komt. In een neutraal milieu is het paars.
|
Tabel: Reacties op zuren en basen van plantaardige stoffen |
||||
|
grondstof |
kleur |
kleur extract |
+ zuur |
+ base |
|
dauwbraam (Rubus caesius) |
blauw |
rood |
rood |
blauw-groen |
|
bosbraam (Rubus fruticosus) |
zwart |
rood |
rood |
blauw-groen |
|
aalbes (rode bes) |
rood |
rood |
rood |
blauw-groen |
|
aardbei |
rood |
oranje |
oranje |
dieprood |
|
rozeboombloem |
rood |
roze |
dieprood |
groen-bruin |
|
chrysantbloem |
geel |
zwakgeel |
geel |
geel |
|
roos |
oranje |
geel |
oranje |
bruin |
|
dubia (bloem) |
paars |
zwakroze |
violet |
frisgroen |
|
fuchsiabloem |
rood |
kleurloos |
violet |
bruin |
|
biet |
rood |
rood |
violet |
lichtbruin |
|
rode kool |
paars/wit |
violet |
dieprood |
frisgroen |

