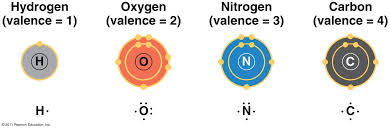
 Zuurstof (Latijn: oxygenium, symbool O, atoomnummer 8) is een niet-metaal dat tot de zuurstofgroep in het Periodiek Systeem behoort. Zuurstof komt als enkelvoudige stof vooral als dizuurstof (O2) in de atmosfeer voor. In samengestelde vorm is het wijdverspreid omdat alle water en alle silicaten waar de aardkorst uit bestaat zuurstof bevatten. Naar gewicht is zuurstof het meest voorkomende element in het menselijk lichaam: ongeveer 65 %, voornamelijk in de vorm van water.
Zuurstof (Latijn: oxygenium, symbool O, atoomnummer 8) is een niet-metaal dat tot de zuurstofgroep in het Periodiek Systeem behoort. Zuurstof komt als enkelvoudige stof vooral als dizuurstof (O2) in de atmosfeer voor. In samengestelde vorm is het wijdverspreid omdat alle water en alle silicaten waar de aardkorst uit bestaat zuurstof bevatten. Naar gewicht is zuurstof het meest voorkomende element in het menselijk lichaam: ongeveer 65 %, voornamelijk in de vorm van water.
Stikstof (symbool N, atoomnummer 7) is een niet-metaal uit de stikstofgroep. Losse atomen hiervan zijn zeer reactief en verbinden zich direct met andere stikstofatomen. Hierbij wordt meestal distikstof gevormd (N2 of moleculaire stikstof), de gangbare verschijningsvorm van stikstof. Op kamertemperatuur verkeert N2 in gasvorm.
Waterstof (symbool H (Latijn: Hydrogenium), atoomnummer 1) komt normaal niet in geïsoleerde vorm voor, maar vormt door de hoge reactiviteit verbindingen. Het vormt een twee-atomig molecule: diwaterstof, meestal gewoon waterstof of waterstofgas genoemd. Waterstof is het meest voorkomende element in het universum. Het normale isotoop van waterstof "protium" bestaat maar uit één proton en één elektron en bevat dus geen neutronen. Waterstof is het enige element dat zonder neutronen bestaat.
Koolstof (symbool C, atoomnummer 6) bestaat in verschillende vormen (houtskool, diamant…) en zit o.m. in koolwaterstoffen (fossiele brandstof), koolhydraten (ethanol, suikers, zetmeel…). Alle organische verbindingen bevatten koolstof. (Enkel CO2 en carbonaten worden toch tot de anorganische stoffen gerekend.) Koolstofverbindingen vormen de basis van al het leven op aarde.
Sacharose, suiker: C12H22O11
Glucose C6H12O6 verbrandt > 6CO2(g) + H2O (g) (omgekeerde = fotosynthese)
Aardgas = methaan CH4 verbrandt CO2 en H2O. Ethaan: H3C-CH3.
Koolhydraten: ((CH2O))n
Alcohol: C2H5OH

